| 分子式 | Al |
| 基质 | 10%HNO3 |
| 形态 | 液体 |
| 存储条件 | 室温、避光保存。 |
| 理化性质 | 铝元素符号Al,原子序数13,原子量26.98,外围电子排布式3s23p1,位于第三周期第Ⅲ A族。金属半径143.1皮米,离子半径51皮米,第一电离能577.4kJ/mol,电负性1.5,氧化数+3。银白色有光泽金属,质轻,有良好的延展性和传热导电性,熔点660.5℃,沸点2467℃,硬度2~2.9,密度2.7g/cm3。丰度(质量%)8.05%,在地壳中居第三位。铝是化学性质较活泼的金属。常温下在空气中金属表面发生缓慢氧化生成一薄层致密氧化物膜,阻止氧气、水继续跟铝反应,但可透过光线,这层膜对铝起保护作用,因此铝有一定抗锈蚀能力。若去掉这层氧化膜,并使铝跟汞形成铝汞齐,则很易被空气中氧气氧化,也能跟水剧烈反应放出氢气生成氢氧化铝。铝在加热时可在氧气中燃烧生成氧化铝发强白光并放出大量的热。由于铝跟氧有较强的亲合力,因此铝有强还原性,冶金工业上用做还原剂,冶炼高熔点金属如镍、铬、锰、钒等,铝粉跟上述金属氧化物粉末的混合物叫铝热剂。用铝还原金属的方法,称为铝热还原法。铝也用做炼钢中的脱氧剂。加热时铝可跟卤素、氮气、磷、硫、碳等化合。高纯铝不跟一般酸反应,只溶于王水。一般铝可溶于盐酸、稀硫酸并放出氢气。常温时在浓硫酸或浓硝酸中发生钝化,因此,可用铝容器储运这些浓酸。铝可跟热硫酸反应放出二氧化硫: 铝可溶于强碱溶液中生成偏铝酸盐并放出氢气。 ???? 2Al+2NaOH+2H2O=2NaAlO2+3H2↑ ?? 纯铝可用于制电线、电缆。铝大量用于制合金、电器设备、建筑设备、机械、化工设备:汽车、飞机、宇航飞行器、日用器皿等。铝粉(俗称“银粉”)用于配制油漆、烟火等。铝在自然界主要以铝硅酸盐的形式存在,如长石、云母、高岭土等。铝矿石主要有铝土矿(Al2O3·nH2O)和冰晶石(Na3AlF6)。1827年德国化学家维勒把无水氯化铝跟钾放在铂坩埚里密闭加热得到粉末状铝。工业上用电解氧化铝跟冰晶石的熔融混合物制得铝。 |
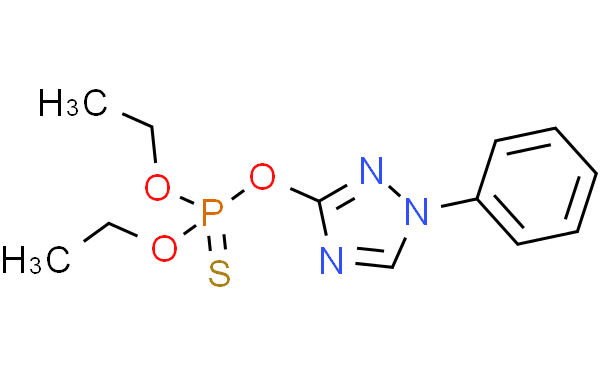 甲醇中三唑磷溶液标准物质
编号:GBW(E)086142 CAS号:24017-47-8 规格:1.2mL 浓度:1000μg/mL
甲醇中三唑磷溶液标准物质
编号:GBW(E)086142 CAS号:24017-47-8 规格:1.2mL 浓度:1000μg/mL
 重铬酸钾滴定溶液标准物质
编号:GBW(E)082928 CAS号:7778-50-9 规格:500mL 浓度:0.25(氧化量浓度C( 1/6K2Cr2O7)(mol/L)(20?C))
重铬酸钾滴定溶液标准物质
编号:GBW(E)082928 CAS号:7778-50-9 规格:500mL 浓度:0.25(氧化量浓度C( 1/6K2Cr2O7)(mol/L)(20?C))
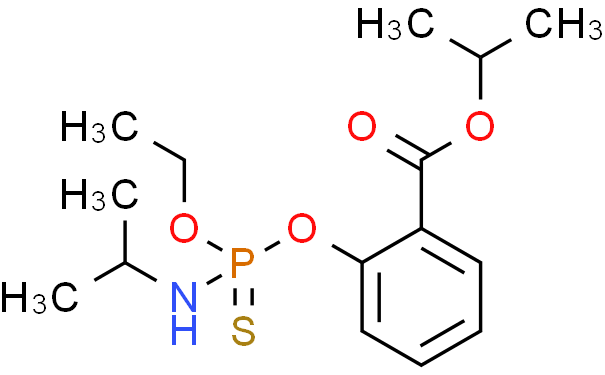 丙酮中异柳磷溶液标准物质
编号:BWN5034-2016 CAS号:25311-71-1 规格:1.2mL 浓度:1000μg/mL
丙酮中异柳磷溶液标准物质
编号:BWN5034-2016 CAS号:25311-71-1 规格:1.2mL 浓度:1000μg/mL
 甲醇中对异丙基甲苯分析校准用标准样品
编号:GSB07-2428-2008 CAS号:99-87-6 规格:1.2mL 浓度:1000μg/ml
甲醇中对异丙基甲苯分析校准用标准样品
编号:GSB07-2428-2008 CAS号:99-87-6 规格:1.2mL 浓度:1000μg/ml
 异戊乙净溶液
编号:1ST22224-100M CAS号:22936-75-0 规格:1mL 浓度:100μg/mL
异戊乙净溶液
编号:1ST22224-100M CAS号:22936-75-0 规格:1mL 浓度:100μg/mL
 苊烯溶液
编号:1ST4302-1000A CAS号:208-96-8 规格:1mL 浓度:1000μg/mL
苊烯溶液
编号:1ST4302-1000A CAS号:208-96-8 规格:1mL 浓度:1000μg/mL